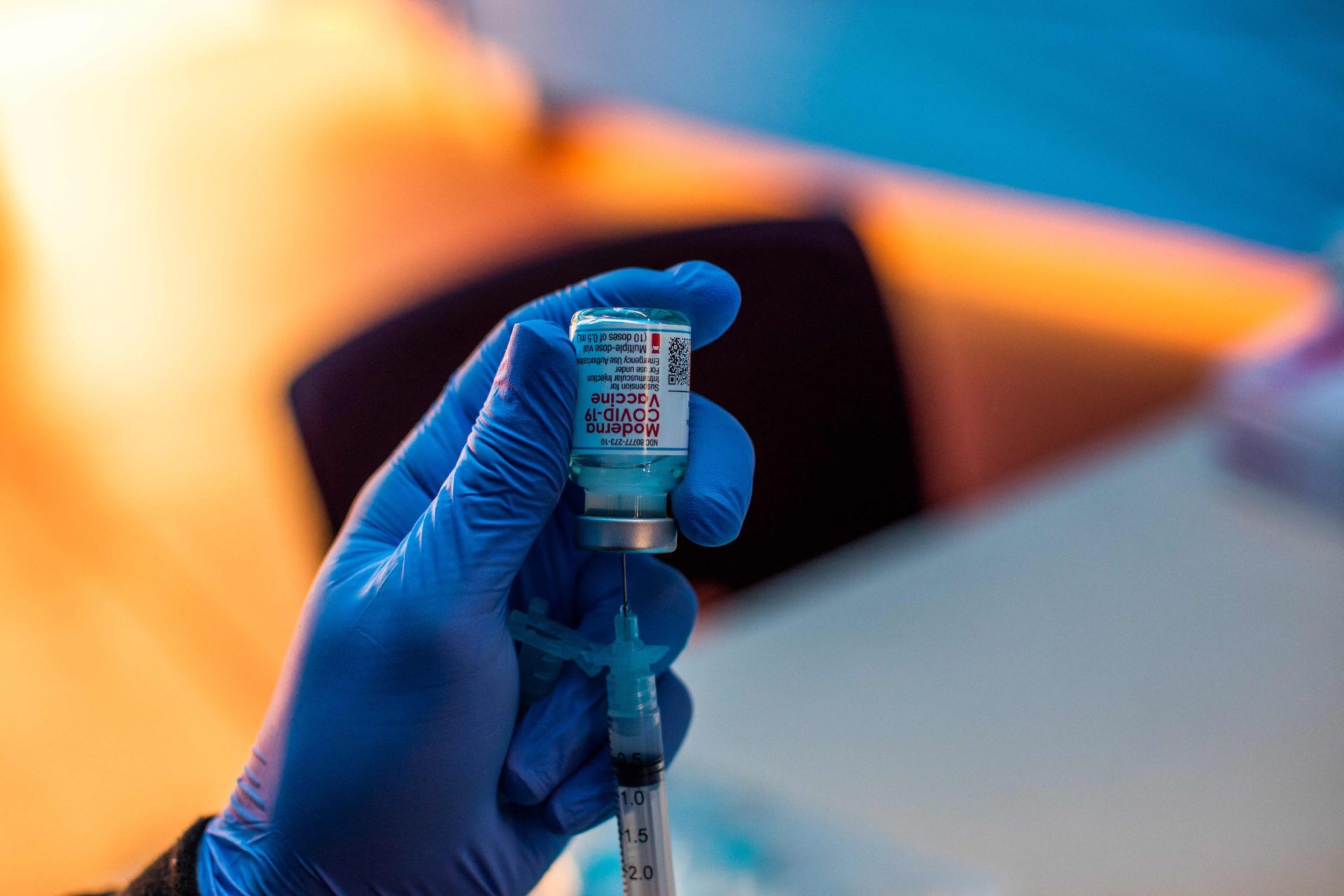
A Agência Europeia do Medicamento (EMA) recomendou, esta quinta-feira, a autorização da inoculação da vacina da farmacêutica Moderna contra a covid-19 em crianças entre os 6 e os 11 anos, bem como a administração das doses de reforço da vacina Comirnaty.
A entidade europeia que regula o setor do medicamento decidiu estender a autorização de uso da Spikevax, que já tinha sido aprovada para adultos e crianças com 12 anos ou mais.
Note-se que a dose que as crianças entre os 6 e os 11 anos, de 50 microgramas, recebem será metade da que foi recomendada para as outras idades, e deverá ser inoculada em duas injeções com quatro semanas de intervalo.
Segundo a EMA, a dose de 50 microgramas produz nas crianças até 11 anos uma reação imunitária comparável à que se verifica com a dose superior em pessoas mais velhas.
O regulador europeu aponta como efeitos secundários mais comuns "dor, vermelhidão e inchaço no local da injeção, cansaço, dores de cabeça, arrepios, vómitos, inchaço dos nódulos linfáticos nas axilas, febre e dores musculares e articulares", acrescentando que são "habitualmente ligeiros ou moderados e melhoram nos dias a seguir à vacinação".
Tendo em conta a semelhança da "eficácia e a segurança da Spikevax" em crianças com idades entre os 6 e os 11 anos e nos adultos, a EMA concluiu que "os benefícios da Spikevax neste grupo etário ultrapassam os riscos", sobretudo em crianças em risco aumentado de contraírem formas graves de covid-19.
Ainda assim, a EMA ressalva que a Spikevax está a ser "monitorizada de perto" e que "embora um grande número de pessoas já tenha recebido vacinas contra a covid-19, alguns efeitos secundários poderão surgir à medida que mais recebem as vacinas".
Já a Moderna tem que dar à autoridade "atualizações regulares e fazer estudos para monitorizar a segurança e a eficácia da vacina", relevou a EMA.
Em relação à vacina Comirnaty, a EMA considerou que uma dose de reforço é adequada em crianças com 12 anos ou mais. Recorde-se que esta vacina já é autorizada na União Europeia para adolescentes, adultos e crianças com 5 anos ou mais e as doses de reforço autorizadas a partir dos 18 anos.
A EMA justifica o seu apoio nesta vacina através de um ensaio clínico de dose de reforço deste fármaco dado a pessoas com 16 ou mais anos e em "literatura publicada e dados pós-autorização, além de dados reais de doses de reforço em jovens em Israel".
"São esperados mais dados de estudos e análises em adolescentes nos próximos meses", realçou ainda a EMA, sublinhando que tal como em recomendações anteriores, caberá aos estados-membros decidir como conduzem as suas campanhas de vacinação.
"A decisão sobre dar reforços nesta faixa etária terá que ter em conta fatores como a propagação e a probabilidade de gravidade da doença, sobretudo com a variante Ómicron, em pessoas mais jovens, o risco conhecido de efeitos secundários, em particular a ocorrência muito rara mas grave de miocardite [uma inflamação do músculo do coração]", sublinhou a EMA.